Mostrando entradas con la etiqueta 4. Enlace químico y estructura de la materia. Mostrar todas las entradas
Mostrando entradas con la etiqueta 4. Enlace químico y estructura de la materia. Mostrar todas las entradas
Espectros de emisión y de absorción de los elementos químicos
1. Antes de nada investiga cómo se obtienen estos espectros. Para ello veremos el dispositivo empleado para ver algunos ejemplos de espectros de emisión y espectros de absorción.
3. Y ahora responde:
- ¿Qué importancia pueden tener estos espectros atómicos?
- ¿Qué información se extrae de los espectros de emisión y de absorción?
- ¿Qué diferencias existen entre ambos tipos de espectros?
Laboratorio de dureza, conductividad eléctrica y solubilidad
Introducción
En el desarrollo de esta unidad hemos repetido muchas veces que los modelos teóricos que describen el enlace químico entre átomos, deben justificar las propiedades de las sustancias. Es hora de someterlos a juicio y comprobar si son (o no) capaces de justificar o predecir las propiedades de las sustancias.
Para ello vamos a realizar pruebas experimentales a diferentes sustancias, anotaremos los resultados y trataremos de justificar las propiedades observadas mediante los modelos estudiados de enlace iónico, covalente o metálico.
Actividades
1. Laboratorio de dureza.  Experimenta en este laboratorio de dureza y ordena los materiales de MAYOR a menor dureza. Para finalizar, completa en tu informe de laboratorio, el tipo de enlace de cada una de las sustancias y la explicación de esta escala de dureza.
Experimenta en este laboratorio de dureza y ordena los materiales de MAYOR a menor dureza. Para finalizar, completa en tu informe de laboratorio, el tipo de enlace de cada una de las sustancias y la explicación de esta escala de dureza. 2. Laboratorio de solubilidad
2. Laboratorio de solubilidadEn este caso debes realizar las actividades que te proponen:
1- Determina la solubilidad de las sustancias A,B,C,D a 25ºC y a 50ºC
2- Dibuja la gráfica solubilidad temperatura para la sustancia D.
Y además:
3.Justificar el tipo de enlace que presentan A, B, C y D en relación con la solubilidad que has observado.
3. Grafeno y sus aplicaciones
El grafeno es un material nuevo de innumerables aplicaciones. Tras ver este vídeo:
Informe de actividades
Tras realizar las actividades propuestas, elabora un documento (en formato pdf) y lo subes según el procedimiento indicado en este blog. Dicho informe será evaluado y discutido en la clase.
El grafeno es un material nuevo de innumerables aplicaciones. Tras ver este vídeo:
- Elabora dos listas de este material:
- aplicaciones científicas y tecnológicas
- propiedades.
- Describe brevemente desde el punto de vista del enlace químico y de su estructura interna, la justificación de estas propiedades
Informe de actividades
Tras realizar las actividades propuestas, elabora un documento (en formato pdf) y lo subes según el procedimiento indicado en este blog. Dicho informe será evaluado y discutido en la clase.
Visualizador de moléculas, biomoléculas,....
Extraordinario visualizador CANVAS que permite exportar imágenes de biomoléculas, moléculas sencillas, estructuras del C y algunos cristales. Por supuesto se pueden mover y crear diferentes modelos:
Adn
Cristal de fluorita
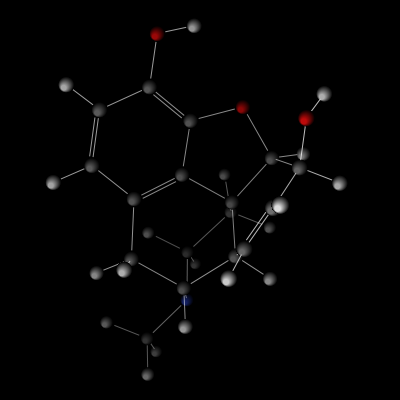
Morfina
C-60
Enlace químico
- Concepto de enlace químico y estabilidad energética
- Enlace iónico
- Propiedades de las sustancia iónicas
- Enlace covalente
- Parámetros moleculares
- Teoría del enlace valencia TEV
- Modelo de repulsión de pares electrónicos en las capas de valencia (RPECV)
- Hibridación
- Propiedades de las sustancias covalentes
- Fuerzas intermoleculares
- Enlace metálico
- Teorías del enlace metálico
- Propiedades de las sustancias metálicas
MAPAS ENCADENADOS DE LA UNIDAD
Argumentando las actividades
FUNDAMENTOS DEL ENLACE QUÍMICO
PRESENTACIÓN DE CLASE
Argumentando las actividades
FUNDAMENTOS DEL ENLACE QUÍMICO
PRESENTACIÓN DE CLASE
Problemas complementarios
Introducción al enlace covalente
1. Tipos de sustancias.
Una web sobre enlace con animaciones microscópicas (Premiada en CNICE)
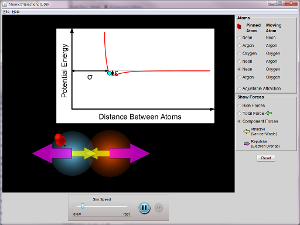
2. Interacciones atractivas y repulsivas que originan las curvas de estabilidad (curvas de Morse) .
3. Características de los enlaces
3. Características de los enlaces
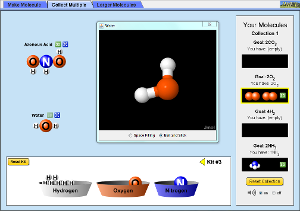
4. Construyendo moléculas.
Fuerzas intermoleculares (no enlace)
Como recordarás existen diferentes interacciones:
- Entre átomos, es decir interatómicas. Son los verdaderos enlaces químicos: iónicos, covalentes o metálicos.
- Interacciones intermoleculares, que engloban a aquellas interacciones de "no enlace". Entre ellas encontramos:
- Enlaces por puentes de hidrógeno. Explican las anomalías en las propiedades físicas, químicas o estructurales de moléculas covalentes que presenten alguno o varios de estos enlaces: H-F, H-O, H-N
- Fuerzas de Van der Waals que aparecen:
- Entre moléculas apolares en las que se pueda inducir un dipolo mediante la formación de un dipolo temporal. A estas las llamaremos fuerzas de dispersión o fuerzas de London. Son las mas débiles de todas, y por ello en muchos casos, incluso a temperatura ambiente si siquera podemos manifestarlas debido a que la agitación molecular las destruye.

 El último caso es la solvatación de iones mediante moléculas polares. Serían interacciones ión-dipolo, que darían lugar a que los iones se rodean de moléculas polares (dipolos permanentes) que se orientan de acuerdo con la carga del ión.
El último caso es la solvatación de iones mediante moléculas polares. Serían interacciones ión-dipolo, que darían lugar a que los iones se rodean de moléculas polares (dipolos permanentes) que se orientan de acuerdo con la carga del ión.Hidridación
Paso 1: Formación de orbitales híbridos en el átomo central
- Híbridos sp: s- p- p- p- (4 OA) dará lugar a sp- sp- p- p- (2 oh + 2oa no hibridados).
- 2 OH sp: disposición lineal (ángulo de 180º)
- 2 OA p, perpendiculares entra si y a los OH sp
- Híbridos sp2: s- p- p- p- (4 OA) dará lugar a sp2- sp2- sp2- p- (3 oh + 1oa no hibridados)
- 3 OH sp2: disposición triangular plana (ángulo de 120º)
- 1 OA p, perpendicular a los híbridos sp2
- Híbridos sp3: s- p- p- p- (4 OA) dará lugar a sp3- sp3- sp3- sp3- (4 oh)
- 4 OH sp3: disposición tetraédrica (ángulo de 109,5º)
Paso 2: Solapamientos de OH con OA de otros átomos o con OH de otros átomos.
Etano
C(OH sp3)- C(OH sp3) = solapamiento sigma
C(OH sp3) - H(OA s) = solapamiento sigma (x3 veces)
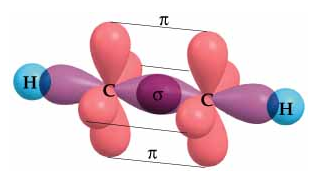
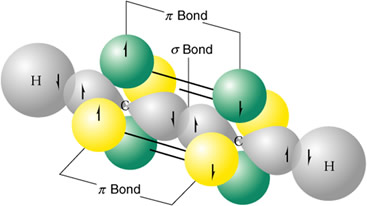
Eteno
C(OH sp2)- C(OH sp2) = solapamiento sigma
C(OA p) - C(OA p) = solapamiento pi
C(OH sp2) - H(OA s) = solapamiento sigma (x2 veces)
Etino
C(OH sp)- C(OH sp) = solapamiento sigma
C(OA p) - C(OA p) = solapamiento pi (x 2 veces en planos perpendiculares)
C(OH sp2) - H(OA s) = solapamiento sigma
Extraordinario vídeo que explica la disposición de orbitales híbridos enlazantes (con ppar de enlace pe) o híbridos con pares de electrones no enlazantes (pne = psolitario = par no compartido).
Hybrid Orbitals in Organic Chemistry from the Wolfram Demonstrations Project by Guenther Gsaller
Geometría molecular por la TRPECV
Fuerzas intermoleculares: "la unión hace la fuerza"
Este vídeo muestra un sorprendente robot pequeñito que es capaz de arrastrar un objeto de un peso 100 veces mayor que el suyo...una vez más el hombre aprende por imitación de la naturaleza.
El fundamento de este sorprendente robot, no es sólo tecnológico, o físico, sino químico, ya que es el mismo que utilizan las salamandras para quedarse "pegadas" en el techo....
La clave está en un tipo de fuerzas intermoleculares, de magnitud muy inferior a cualquier enlace químico.
Estas fuerzas tan débiles, llamadas fuerzas de Van der Waals, tiene carácter eléctrico, se producen por la aparición de "cargas temporales" en la superficie molecular, es decir por la formación de dipolos temporales que actúan entre sí. Quizá lo más importante es que estas fuerzas, se multiplican cuando aumenta la superficie de contacto, es decir cuando "la unión hace la fuerza".
Polaridad de un enlace, polaridad molecular y geometría molecular
1. POLARIDAD DE UN ENLACE
El momento dipolar de un enlace depende pues de dos factores:
- Carga que soporta cada átomo enlazado (separación de carga originada por la diferencia de electronegatividad)
- Distancia entre los átomos enlazados. En ocasiones este factor será opuesto al anterior, pero será menos relevante frente a la separación de carga originada por la diferencia de electronegatividad.
Viene determinada por la suma vectorial de los momentos dipolares de enlace
Por ello, hay que tener cuidado de los aspectos siguientes:
- ¿Son iguales entre si?
- ¿Están simétricamente distribuidos en el espacio?
Suscribirse a:
Entradas (Atom)